O texto da decisão, da juíza federal Daniela Pereira Madeira, do Rio de Janeiro, diz que a patente, que protegeria os direitos da empresa farmacêutica Abbott de produzir o medicamento com exclusividade até 2016, não é válida.
Os motivos para isso seriam a falta da avaliação da Anvisa (Agência Nacional de Vigilância Sanitária) antes da concessão da patente e a inconstitucionalidade do método de registro, o chamado "pipeline". Estabelecido em 1996, o método revalidava automaticamente no país as patentes registradas no exterior.
Em 1999, foi introduzida a exigência de que os pedidos de registro fossem analisados pela Anvisa, o que não foi feito no caso do antirretroviral.
O pedido de patente do Kaletra já havia sido iniciado antes disso, mas só foi concedido depois, em 2000. Por isso, entendeu-se que deveria ter passado pela agência.
A revalidação pelo "pipeline" seria inconstitucional porque concedeu monopólio de produção a um medicamento que já estava em domínio público, segundo o advogado Alexandre Serafim, da equipe que representou o laboratório Cristália, autor do processo. "Quando o pedido de patente foi iniciado, o Brasil não reconhecia patentes de remédios. O pipeline deu monopólio sobre moléculas em domínio público."
O advogado Lucas de Moura Gavião, que também atuou no processo, diz que há outros remédios nessa situação e que essa ação pode criar um precedente.
A decisão é em primeira instância e pode ser contestada pela Abbott.
| Editoria de arte/Folhapress | ||
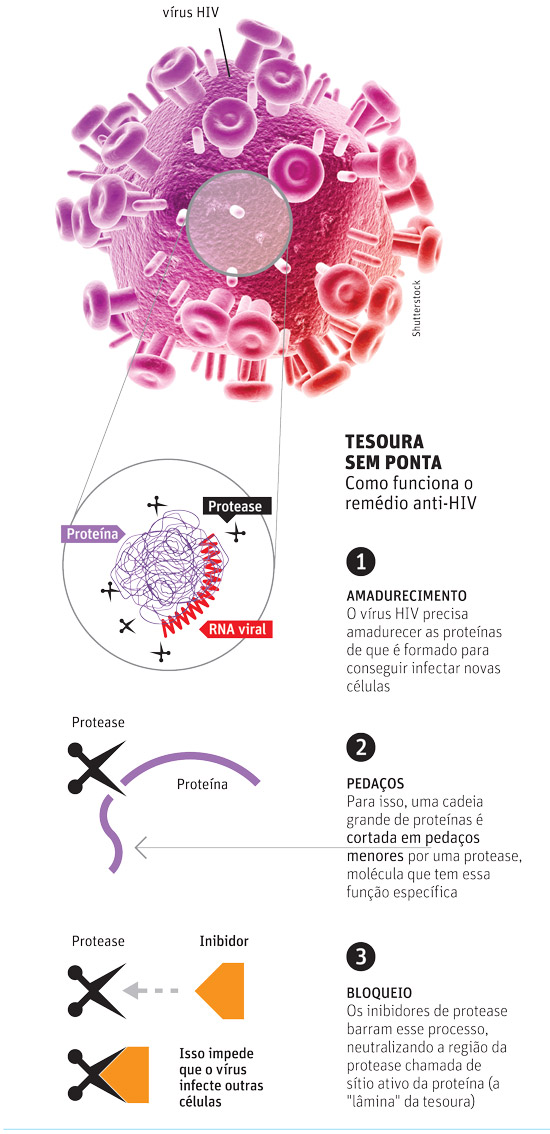 |
Em 2011, segundo informações do Ministério da Saúde, foram gastos R$ 91 milhões em compras do medicamento. Os gastos totais do governo com antirretrovirais, que foram de R$ 1 bilhão em 2005, caíram nos anos seguintes, após negociações de preço com as fabricantes e licenciamento compulsório de remédios. Em 2007, o valor total foi de R$ 710 milhões.
O presidente do laboratório Cristália, Ogari Pacheco, diz que a empresa entrou com a ação porque tem capacidade técnica de produzir a droga, composta pelos princípios ativos ritonavir e lopinavir.
"Agora que a patente caiu, poderemos produzir a associação de medicamentos a preços competitivos em nível mundial", afirma Pacheco, que diz que é cedo para falar em valores exatos.
O infectologista Caio Rosenthal afirma que o medicamento é importante no combate ao HIV. "A indústria já teve retorno suficiente de seu investimento em pesquisa. Não há mais por que manter preços abusivos sobre remédios contra o HIV", diz o médico, do Instituto de Infectologia Emílio Ribas.
OUTRO LADO
A Abbott, fabricante do Kaletra, enviou nota à reportagem dizendo que defende da validade da patente. "Estamos analisando as medidas legais cabíveis."
Antônio Britto, presidente-executivo da Interfarma (Associação da Indústria Farmacêutica de Pesquisa) afirma que o Brasil tem um ambiente de segurança jurídica quanto à validade das patentes e que o setor aguarda com tranquilidade os próximos passos do processo. "Em 15 anos, podemos contar nos dedos os casos de processo. A legislação no país é boa."
Para Britto, o caso não deve dar base a novas contestações de patentes
DÉBORA MISMETTI
Folha
KALETRA: Lopinavir / ritonavir
| Combinação de | |
|---|---|
| Lopinavir | Inibidor da protease |
| Ritonavir | Inibidor da protease |
AcessoComo resultado dos elevados preços e da propagação da infecção pelo HIV, o governo da Tailândia emitiu uma licença compulsória em 29 de janeiro de 2007, para produzir e / ou importação de genéricos versões de lopinavir e ritonavir. [8] Em resposta, a Abbott Laboratories retirou seu registro de lopinavir e sete de seus outros novos medicamentos na Tailândia, alegando falta do governo tailandês de respeito para patentes . [9] atitude Abbott tem sido denunciado por vários ONGs em todo o mundo, incluindo um netstrike iniciado por Act Up-Paris e uma chamada pública para boicotar todos os medicamentos da Abbott pela ONG francesa AIDES | |
| Lopinavir / ritonavir ( DCI ) é uma combinação de dose fixa de drogas para o tratamento de HIV infecção. Combina lopinavir (não disponível como uma única droga) com uma dose sub-terapêutica de ritonavir (comércio Norvir nome) em um comprimido de dose fixa. A combinação é comercializado pela Abbott como Kaletra (países de alta renda) e Aluvia (países de baixa renda), como um componente da terapia de combinação para o tratamento de HIV / AIDS . A formulação Kaletra também tem sido utilizado com sucesso como monoterapia em alguns estudos. [1] A partir de 2006, o lopinavir / ritonavir faz parte da combinação preferida para terapia de primeira linha recomendado por os EUA DHHS . [2] Ele está disponível como cápsulas, comprimidos e solução oral. | |
História
Lopinavir foi desenvolvido por Abbott , numa tentativa de melhorar a resistência do HIV e séricos da proteína de ligação de propriedades de inibidor da empresa protease anteriormente, ritonavir. [3] administrado sozinho, lopinavir tem biodisponibilidade insuficiente, no entanto, como inibidores da protease vários HIV, o sangue a sua níveis são grandemente aumentadas por doses baixas de ritonavir, um potente inibidor da citocromo P450 3A4 . [3] Abbott, por conseguinte, prosseguiu uma estratégia de co-administração de lopinavir com sub-doses terapêuticas de ritonavir e lopinavir só é comercializado como um co-formulação com ritonavir. É a cápsula multi-droga primeiro para conter uma droga não disponível individualmente.Lopinavir / ritonavir foi aprovado pelos EUA FDA em 15 de Setembro de 2000, e na Europa em Abril de 2001. A sua patente expirará em os EUA em 26 de junho de 2016.
Abbott Laboratories foi um dos primeiros usuários do Advanced Photon Source , uma fonte de luz síncrotron nacional radiação em Argonne National Laboratory . Um dos primeiros projetos de pesquisa realizados no Advanced Photon Source foi o Vírus da Imunodeficiência Humana. Usando cristalografia de raios X , os investigadores descobriram os pontos de ataque dos inibidores da protease do HIV-agentes que bloqueiam a degradação de proteínas. Os inibidores de protease de HIV de fazer parar novas cópias de si através do bloqueio da última etapa do processo, quando o vírus tenta replicar - e para fora do veio que a descoberta de que a droga Kaletra. [4]
Os efeitos adversos
Os efeitos adversos mais comuns observados com lopinavir / ritonavir são diarréia e náuseas . Nos principais ensaios clínicos, diarréia moderada ou grave ocorreu em até 27% dos pacientes, e moderada / severa, náuseas em até 16%. [5] Outros efeitos adversos comuns incluem dor abdominal , astenia , dor de cabeça , vômitos e, particularmente em crianças , erupção cutânea . [5]Enzimas hepáticas elevadas e hiperlipidemia (ambos hipertrigliceridemia e hipercolesterolemia ) também são comumente observados durante o lopinavir / ritonavir tratamento.
Pacientes com estrutural doença cardíaca , doenças preexistentes, anormalidades de condução do sistema, doença isquêmica do coração , ou cardiomiopatias deve usar lopinavir / ritonavir com cautela. [6]
Em 8 de março de 2011 os EUA Food and Drug Administration notificou os profissionais de saúde de sérios problemas de saúde que têm sido relatados em bebês prematuros que receberam lopinavir / ritonavir solução oral, provavelmente por causa de sua propilenoglicol conteúdo. Eles recomendam o uso deve ser evitado em bebês prematuros. [7]
Origem: Wikipédia, a enciclopédia livre
.

Nenhum comentário:
Postar um comentário